Как вылечить дилатационную кардиомиопатию
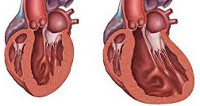
Дилатационная кардиомиопатия как правило возникает без видимой причины и вскоре начинает казаться приговором – причины возникновения неизвестны, лечение преимущественно симптоматическое, состояние постепенно ухудшается, прогноз неутешительный.
Что может предложить современная медицина для лечения кардиомиопатии?
Мало кому известно, что современная медицина может предложить нечто большее, чем поддерживающая терапия, и у пациентов с кардиомиопатией есть реальный шанс не только остановить развитие болезни, но в значительной степени улучшить свое самочувствие и вернуть себе удовольствие от жизни.
Как лечить дилатационную кардиомиопатию?
До недавнего времени единственным радикальным способом лечения дилатационной кардиомиопатии была пересадка сердца. Из-за несовершенства системы донорства органов и небольшого числа клиник и специалистов, занимающихся трансплантацией органов, таких операций в России делается крайне мало – за 25 летнюю историю отечественной трансплантологии было пересажено всего около 350 сердец. Нуждающихся же в донорском сердце пациентов гораздо больше.
При этом лечение за рубежом стоит астрономических денег и тоже зависит от наличия подходящего донора. Поэтому время ожидания нового сердца зачастую превышает срок жизни пациента, несмотря на проводимую лекарственную терапию.
Есть ли альтернативный метод лечения?
Однако в настоящее время медицина может предложить альтернативный выход – улучшить состояние пораженного миокарда (сердечной мышцы), используя собственные возможности организма пациента. Такую возможность дает лечение стволовыми клетками.
Умные клетки
При дилатационной кардиомиопатии сердечная мышца становится “дряблой” и истонченной, из-за чего полости сердца увеличиваются в размерах и орган все хуже справляется со своей основной функцией – перекачиванием крови. В результате этого ухудшается кровоснабжение всех органов. Кроме того, из-за замедления кровотока в тканях и полостях тела скапливается излишняя жидкость, что проявляется выраженными отеками и одышкой.
Как остановить патологические изменения в миокарде и улучшить состояние?
Затормозить патологические изменения в миокарде и улучшить его состояние и функции позволяет введение мезенхимальных стволовых клеток. Эти клетки не обладают признаками какой-либо определенной ткани организма, являясь “универсальными”. Они обладают двумя важнейшими особенностями – возможностью к размножению с сохранением этой универсальности и способностью развиваться в клетки разных тканей, таких как сердечная мышца, соединительная ткань, сосуды и нервы, необходимые для всестороннего восстановления поврежденного органа.
Эти особенности стволовых клеток позволяют использовать их в лечении ряда заболеваний, в том числе дилатационной кардиомиопатии. Такое лечение включает несколько этапов.
Первый этап лечения: обследование
Сначала пациента подвергают всестороннему обследованию, чтобы точно выяснить, подходит ли ему терапия стволовыми клетками и каких можно ожидать результатов. Когда обследование завершено, у человека в амбулаторных условиях забирают небольшой образец костного мозга или жировой ткани и выделяют из него мезенхимальные стволовые клетки.
Второй этап лечения: стволовые клетки
Затем полученные клетки на срок от двух до четырех недель помещают в инкубатор для получения нужного их количества: для лечения необходимо не менее 100 миллионов клеток плюс некоторое их число консервируют (замораживают при температуре жидкого азота) и сохраняют в криобанке на случай повторной терапии в будущем.
Третий этап лечения: превращение в кардиомиобласты
После выращивания в инкубаторе у части клеток с помощью стандартизованных химических стимулов вызывают частичную дифференцировку – превращение в кардиомиобласты (предшественники мышечных волокон сердца, сохраняющие частичную универсальность).
Четвертый этап лечения: ввод клеток
Полученную в итоге смесь необходимого количества мезенхимальных стволовых клеток и кардиомиобластов вводят пациенту внутривенно. С током крови эти клетки попадают в сердце, распознают повреждение (такая способность заложена во всех стволовых клетках) и начинают работу.
Что происходит с клетками?
Сначала клетки интенсивно размножаются – через небольшой промежуток времени их количество измеряется триллионами. Затем они начинают развиваться в необходимые для компенсации повреждений ткани. Особенно интенсивно происходит рост новых сосудов, снабжающих миокард кровью.
В течение этого процесса введенные клетки выделяют специфические сигнальные молекулы, которые активируют собственные стволовые клетки сердца, мобилизуя их на борьбу с заболеванием.
Результат процедуры ввода стволовых клеток и кардиомиобластов
В результате этого повышается прочность, эластичность и работоспособность сердечной мышцы, что видно по улучшению таких показателей как конечные систолический и диастолический объемы камер сердца, фракция выброса и усвоение кислорода миокардом.
Субъективно это проявляется улучшением общего состояния, уменьшением отеков и одышки, повышением работоспособности и, как следствие, возможностью вести более полноценную жизнь.
Редакция благодарит московскую Клинику стволовых клеток “Новейшая медицина”.
Источник
Лекарственное лечение дилатационной кардиомиопатии
Учитывая, что ведущим клиническим синдромом при дилатационной кардиомиопатии служит сердечная недостаточность, то в основу лечения должно быть положено назначение ингибиторов АПФ и диуретиков. Ингибиторы АПФ не только увеличивают фракцию выброса левого желудочка, повышают толерантность больных к физической нагрузке и в некоторых случаях улучшают функциональный класс недостаточности кровообращения, но и улучшаю) прогноз жизни, снижают смертность, повышают выживаемость у больных с низкой фракцией выброса. Поэтому ингибиторы АПФ – препараты первого ряда при лечении больных с ХСН. Назначение этих средств показано на всех стадиях симптоматической сердечной недостаточности, связанной с систолической дисфункцией миокарда.
По некоторым данным, бета-адреноблокаторы улучшают прогноз и общее состояние больного. Лечение рекомендуется начинать с малых доз. Препараты из группы бета-адреноблокаторов, воздействуя на гиперактивацию симпатоадреналовой системы, показали способность улучшать гемодинамику и течение сердечной недостаточности, оказывать протективное действие на кардиомиоциты, снижать тахикардию и предотвращать нарушения ритма.
Лечение сердечной недостаточности следует проводить в соответствии с Национальными рекомендациями по диагностике и лечению ХСН.
Злокачественные желудочковые аритмии – ведущая причина внезапной сердечной смерти у пациентов с дилатационной кардиомиопатей. Однако у больных с далеко зашедшей формой болезни причинами до 50% случаев остановки сердца могут быть брадиаритмии, эмболии легочной артерии и других сосудов, электромеханическая диссоциация. Рабочей группой по изучению внезапной смерти при Европейском обществе кардиологов (2001) рекомендовано использовать следующие маркеры внезапной смерти при дилатационной кардиомиопатии:
- устойчивая желудочковая тахикардия (I класс доказательности);
- синкопальные состояния (I класс доказательности);
- снижение фракции выброса левого желудочка (IIа класс доказательности);
- неустойчивая желудочковая тахикардия (IIВ класс доказательности);
- индукция желудочковой тахикардии при электрофизиологи песком исследовании (III класс доказательности).
При синусовой тахикардии симптоматическое лечение проводят бета-адреноблокаторами или верапамилом, начиная с минимальных доз.
Пациенты с желудочковой экстрасистолией имеют повышенный риск внезапной смерти, однако противоаритмические средства не улучшают прогноз при бессимптомном ее течении с диагнозом «ДКМП» или при наличии лишь сердцебиения, В случае симптомов левожелудочковой недостаточности к лечению добавляют бета-адреноблокаторы. При желудочковой экстрасистолии высоких градаций используют амиодарон, соталол, антиаритмические препараты Iа класса.
При наличии желудочковой тахикардии и гемодинамически значимых нарушений (обмороков, пресинкопальных состояний, артериальной гипотензии) следует предполагать неблагоприятный прогноз заболевания. Рекомендуется назначать лечение амиодароном, уменьшающим смертность на 10-19% у пациентов с высоким риском внезапной смерти, а также надо рассмотреть необходимость имплантации кардиовертера или дефибриллятора, У больных с устойчивой желудочковой тахикардией и дилатационной кардиомиопатией при невозможности трансплантации сердца основным методом лечения служит имплантация кардиовертера или дефибриллятора.
Выбор метода купирования пароксизма желудочковой тахикардии определяется но состоянию гемодинамики: если она нестабильна, то проводят синхронизированную кардиоверсию (мощность разряда 200 Дж), При стабильной гемодинамике рекомендуется внутривенное введение лидокаина (болюс + непрерывная инфузия). При отсутствии эффекта прибегают к введению амиодарона или прокаинамида. Если желудочковая тахикардия сохраняется, то проводят синхронизированную кардиоверсию (мощность разряда 50-100 Дж).
При фибрилляции предсердий тактика лечения зависит от ее формы (пароксизмальная, персистируюшая, постоянная). Так, при развитии пароксизмальной фибрилляции предсердий и наличии частого желудочкового ритма, признаков сердечной недостаточности, которые быстро не реагируют на фармакологические средства, показана немедленная электрическая кардиоверсия. Медикаментозная или электрическая кардиоверсия для быстрого восстановления синусового ритма показана у больных с впервые обнаруженным эпизодом фибрилляции предсердий. У пациентов с кардиомегалией, т.е. ДКМП, восстановление синусового ритма при постоянной форме фибрилляции предсердий противопоказано, При неэффективности медикаментозной или электрической кардиоверсии осуществляется контроль частоты желудочковых сокращений в сочетании с антитромботическим лечением [показано в случае фибрилляции предсердий и нарушения функции левого желудочка (наличие хронической сердечной недостаточности, фракция выброса левого желудочка менее 35%)], Для контроля ЧСС при постоянной форме фибрилляции предсердий более эффективна комбинация сердечных гликозидов и бета-адрепоблокаторов.
Хирургическое лечение дилатационной кардиомиопатии
Хирургическое лечение дилатационной кардиомиопатии (трансплантация сердца, кардиомиопластика, применение искусственного левого желудочка) показано при неэффективности медикаментозного, но выполняется редко, главным образом пациентам молодого и среднего возраста.
Трансплантация сердца показана при прогрессирующе нарастающей сердечной недостаточности и если ДКМП развилась у больного моложе 60 лет.
Главная альтернатива трансплантации сердца на сегодняшний день – применение аппаратов вспомогательного кровообращения, которые получили название искусственных желудочков сердца.
Источник
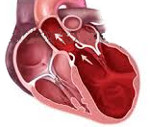
Дилатационная кардиомиопатия – это миокардиальное поражение, характеризующееся расширением полости левого или обоих желудочков и нарушением сократительной функции сердца. Дилатационная кардиомиопатия проявляется признаками застойной сердечной недостаточности, тромбоэмболическим синдромом, нарушениями ритма. Диагностика дилатационной кардиомиопатии основывается на данных клинической картины, объективного обследования, ЭКГ, фонокардиографии, ЭхоКГ, рентгенографии, сцинтиграфии, МРТ, биопсии миокарда. Лечение дилатационной кардиомиопатии проводится ингибиторами АПФ, β-адреноблокаторами, диуретиками, нитратами, антикоагулянтами и антиагрегантами.
Общие сведения
Дилатационная кардиомиопатия (застойная, конгестивная кардиомиопатия) – клиническая форма кардиомиопатии, в основе которой лежит растяжение полостей сердца и систолическая дисфункцией желудочков (преимущественно левого). В современной кардиологии на долю дилатационной кардиомиопатии приходится около 60% всех кардиомиопатий. Дилатационная кардиомиопатия чаще манифестирует в возрасте 20-50 лет, однако встречается у детей и пожилых людей. Среди заболевших преобладают лица мужского пола (62-88%).

Дилатационная кардиомиопатия
Причины дилатационной кардиомиопатии
В настоящее время существует несколько теорий, объясняющих развитие дилатационной кардиомиопатии: наследственная, токсическая, метаболическая, аутоиммунная, вирусная. В 20–30 % случаев дилатационная кардиомиопатия является семейным заболеванием, чаще с аутосомно-доминантным, реже – с аутосомно-рецессивным или Х-сцепленным (синдром Барта) типом наследования. Синдром Барта, кроме дилатационной кардиомиопатии, характеризуется множественными миопатиями, сердечной недостаточностью, фиброэластозом эндокарда, нейтропенией, задержкой роста, пиодермиями. Семейные формы дилатационной кардиомиопатии и имеют наиболее неблагоприятное течение.
В анамнезе у 30% пациентов с дилатационной кардиомиопатией отмечается злоупотребление алкоголем. Токсическое воздействие этанола и его метаболитов на миокард выражается в повреждении митохондрий, уменьшении синтеза сократительных белков, образовании свободных радикалов и нарушении метаболизма в кардиомиоцитах. Среди других токсических факторов выделяют профессиональный контакт со смазочными материалами, аэрозолями, промышленной пылью, металлами и пр.
В этиологии дилатационной кардиомиопатии прослеживается влияние алиментарных факторов: недостаточного питания, дефицита белка, гиповитаминоза В1, нехватки селена, дефицита карнитина. На базе этих наблюдений основывается метаболическая теория развития дилатационной кардиомиопатии. Аутоиммунные нарушения при дилатационной кардиомиопатии проявляются наличием органоспецифических кардиальных аутоантител: антиактина, антиламинина, антимиозина тяжелых цепей, антител к митохондриальной мембране кардиомиоцитов и др. Однако аутоиммунные механизмы являются лишь следствием фактора, который пока не установлен.
С помощью молекулярно-биологических технологий (в т. ч. ПЦР) в этиопатогенезе дилатационной кардиомиопатии доказана роль вирусов (энтеровируса, аденовируса, вируса герпеса, цитомегаловируса). Часто дилатационная кардиомиопатия служит исходом вирусного миокардита.
Факторами риска послеродовой дилатационной кардиомиопатии, развивающейся у ранее здоровых женщин в последнем триместре беременности или вскоре после родов, считаются возраст старше 30 лет, негроидная раса, многоплодная беременность, наличие в анамнезе более 3-х родов, поздний токсикоз беременности.
В некоторых случаях этиология дилатационной кардиомиопатии остается неизвестной (идиопатическая дилатационная кардиомиопатия). Вероятно, дилатация миокарда возникает при воздействии ряда эндогенных и экзогенных факторов, преимущественно у лиц с генетической предрасположенностью.
Патогенез
Под действием причинных факторов уменьшается количество функционально полноценно кардиомиоцитов, что сопровождается расширением камер сердца и снижением насосной функции миокарда. Дилатация сердца приводит к диастолической и систолической дисфункции желудочков и обусловливает развитие застойной сердечной недостаточности в малом, а затем и в большом круге кровообращения.
На начальных стадиях дилатационной кардиомиопатии компенсация достигается благодаря действию закона Франка–Старлинга, увеличению ЧСС и уменьшению периферического сопротивления. По мере истощения резервов сердца прогрессирует ригидность миокарда, нарастает систолическая дисфункция, уменьшается минутный и ударный объем, нарастает конечное диастолическое давление в левом желудочке, что приводит к еще большему его расширению.
В результате растяжения полостей желудочков и клапанных колец развивается относительная митральная и трикуспидальная недостаточность. Гипертрофия миоцитов и формирование заместительного фиброза приводят к компенсаторной гипертрофии миокарда. При уменьшении коронарной перфузии развивается субэндокардиальная ишемия.
Вследствие снижения сердечного выброса и уменьшения почечной перфузии активизируются симпатическая нервная и ренин-ангиотензиновая системы. Выброс катехоламинов сопровождается тахикардией, возникновением аритмий. Развивающиеся периферическая вазоконстрикция и вторичный гиперальдостеронизм приводят к задержке ионов натрия, увеличению ОЦК и развитию отеков.
У 60 % пациентов с дилатационной кардиомиопатией в полостях сердца формируются пристеночные тромбы, вызывающие в дальнейшем развитие тромбоэмболического синдрома.
Симптомы дилатационной кардиомиопатии
Дилатационная кардиомиопатия развивается постепенно; длительное время жалобы могут отсутствовать. Реже она манифестирует подостро, после ОРВИ или пневмонии. Патогномоничными синдромами дилатационной кардиомиопатии являются сердечная недостаточность, нарушения ритма и проводимости, тромбоэмболии.
Клинические проявления дилатационной кардиомиопатии включают быструю утомляемость, одышку, ортопноэ, сухой кашель, приступы удушья (сердечная астма). Около 10 % пациентов предъявляют жалобы на ангинозные боли – приступы стенокардии. Присоединение застойных явлений в большом круге кровообращения характеризуется появлением тяжести в правом подреберье, отеков ног, асцита.
При нарушениях ритма и проводимости возникают пароксизмы сердцебиения и перебоев в работе сердца, головокружение, синкопальные состояния. В некоторых случаях дилатационная кардиомиопатия впервые заявляет о себе тромбоэмболией артерий большого и малого кругов кровообращения (ишемический инсульт, ТЭЛА), что может послужить причиной внезапной смерти больных. Риск эмболии увеличивается при мерцательной аритмии, которая сопутствует дилатационной кардиомиопатии в 10—30% случаев.
Течение дилатационной кардиомиопатии может быть быстро прогрессирующим, медленно прогрессирующим и рецидивирующим (с чередованием обострений и ремиссий заболевания). При быстро прогрессирующем варианте дилатационной кардиомиопатии терминальная стадия сердечной недостаточности наступает в течение 1,5 лет от появления первых признаков заболевания. Чаще всего встречается медленно прогрессирующее течение дилатационной кардиомиопатии.
Диагностика
Диагностика дилатационной кардиомиопатии представляет существенные трудности ввиду отсутствия специфических критериев. Диагноз устанавливается путем исключения других заболеваний, сопровождающихся дилатацией полостей сердца и развитием недостаточности кровообращения.
Объективными клиническими признаками дилатационной кардиомиопатии служат кардиомегалия, тахикардия, ритм галопа, шумы относительной недостаточности митрального и трикуспидального клапанов, увеличение ЧД, застойные хрипы в нижних отделах легких, набухание вен шеи, увеличение печени и др. Аускультативные данные подтверждаются с помощью фонокардиографии. Инструментальная диагностика:
- Электрокардиография. На ЭКГ выявляются признаки перегрузки и гипертрофии левого желудочка и левого предсердия, нарушения ритма и проводимости по типу фибрилляции предсердий, мерцательной аритмии, блокады левой ножки пучка Гиса, АВ – блокады. С помощью ЭКГ-мониторирования по Холтеру определяются угрожающие для жизни аритмии и оценивается суточная динамику процессов реполяризации.
- УЗИ сердца. Эхокардиография позволяет обнаружить основные дифференциальные признаки дилатационной кардиомиопатии – расширение полостей сердца, уменьшение фракции выброса левого желудочка. При ЭхоКГ исключаются другие вероятные причины сердечной недостаточности – постинфарктный кардиосклероз, пороки сердца и т. д.; обнаруживаются пристеночные тромбы и оценивается риск развития тромбоэмболии.
- Радиологическая диагностика. Рентгенологически может выявляться увеличение размеров сердца, гидроперикард, признаки легочной гипертензии. Для оценки структурных изменений и сократительной способности миокарда выполняются сцинтиграфия, МРТ, ПЭТ сердца.
- Биопсия миокарда. Используется для дифференциальной диагностики дилатационной кардиомиопатии с другими формами заболевании.
Лечение дилатационной кардиомиопатии
Лечебная тактика при дилатационной кардиомиопатии заключается в коррекции проявлений сердечной недостаточности, нарушений ритма, гиперкоагуляции. Больным рекомендуется постельный режим, ограничение потребления жидкости и соли.
Медикаментозная терапия сердечной недостаточности включает назначение ингибиторов АПФ (эналаприла, каптоприла, периндоприла и др.), диуретиков (фуросемида, спиронолактона). При нарушениях ритма сердца используются b-адреноблокаторы (карведилол, бисопролол, метопролола), с осторожностью – сердечные гликозиды (дигоксин). Целесообразен прием пролонгированных нитратов (венозных вазодилататоров – изосорбида динитрата, нитросорбида), снижающих приток крови к правым отделам сердца.
Профилактика тромбоэмболических осложнений при дилатационной кардиомиопатии проводится антикоагулянтами (гепарин подкожно) и антиагрегантами (ацетилсалициловая кислота, пентоксифиллин, дипиридамол). Радикальное лечение дилатационой кардиомиопатии подразумевает проведение трансплантации сердца. Выживаемость свыше 1 года после пересадки сердца достигает 75–85 %.
Прогноз и профилактика
В целом течение дилатационной кардиомиопатии неблагоприятное: 10-летняя выживаемость составляет от 15 до 30%. Средняя продолжительность жизни после появления симптомов сердечной недостаточности составляет 4–7 лет. Гибель пациентов в большинстве случаев наступает от фибрилляции желудочков, хронической недостаточности кровообращения, массивной легочной тромбоэмболии.
Рекомендации кардиологов по профилактике дилатационной кардиомиопатии включают медико-генетическое консультирование при семейных формах заболевания, активное лечение респираторных инфекций, исключение употребления алкоголя, сбалансированное питание, обеспечивающее достаточное поступление витаминов и минералов.
Источник
